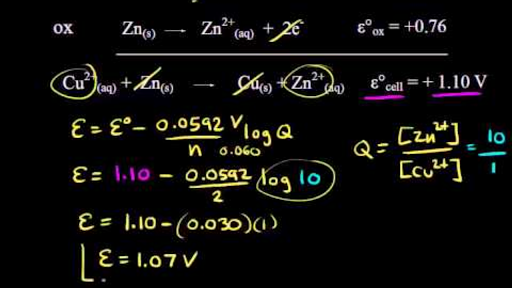1.- Iones en disolución 2.- Reacciones Redox 3.- Celdas Electroquímicas 4.- Potencial de una celda. Ecuación de Nernst 5.- Po

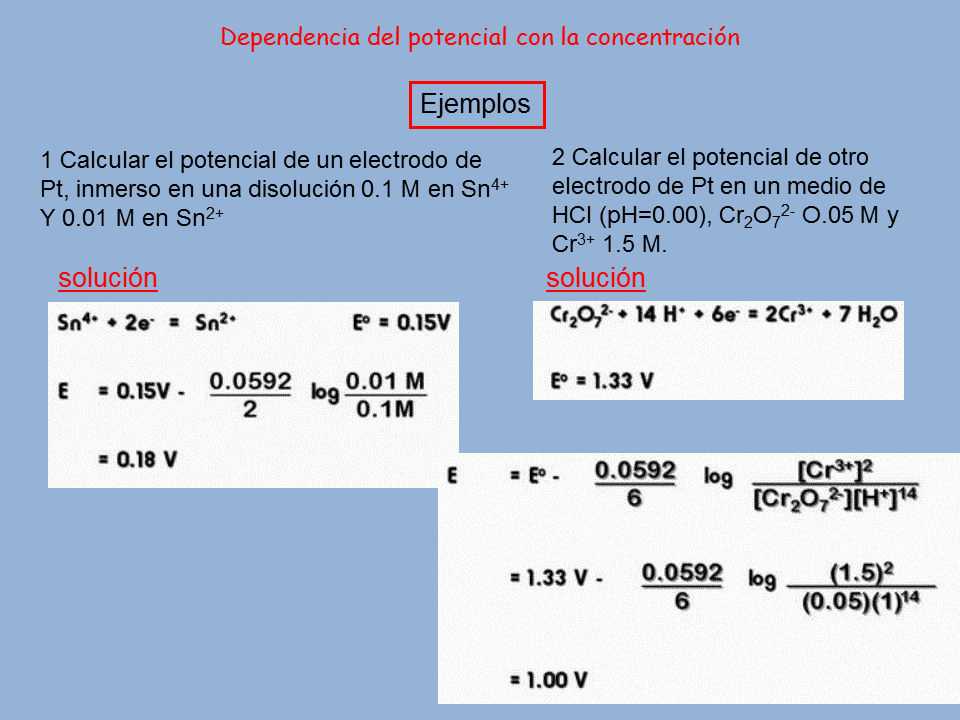
Hasta ahora hemos calculado el potencial de la pila en condiciones estándar. En este apartado aprenderemos a calcularla en otras condiciones, por ejemplo, cuando las concentraciones de las sustancias que intervienen son distintas a 1 M.